Реферат: Алкадиены. Каучук
МПС РФ
ЧИПС УрГУПС
Самостоятельная работа по теме:
«Алкадиены. Каучук»
Выполнил:
студент 17А группы
отд. ОПУД
Шарманов
Владимир
Челябинск
2000
План:
1. Строение
алкадиенов:
а)
молекулярное
б)
структурное
2.
Вид гибридизации
3.
Гомологический ряд
4.
Изомерия
5.
Свойства:
а)
химические
б)
физические
6.
Получение
7.
Применение
Алкадиены,
или диеновые углеводороды, — непредельные углеводороды, содержащие в
углеродной цепи молекулы две двойные связи.
1. Строение
алкадиенов:
а) молекулярное
C4H6 – бутадиен
C5H8 - пентадиен
б) структурное
CH2 =
CH – CH = CH2
бутадиен-1,3
CH2 =
CH – CH = CH2
|
CH3
2-метилбутадиен-1,3
2. Вид
гибридизации
CH2 =
CH – CH = CH2
бутадиен-1,3
Атомы
углерода в молекуле бутадиена-1,3 находятся в состоянии sp3-гибридизации.
За счет гибридных sp3-орбиталей,
оси симметрии которых лежат в одной плоскости, в молекуле возникают s-связи между всеми атомами углерода и s-связи углерод
– водород. Центры всех атомов в молекуле бутадиена-1,3 лежат в одной плоскости.
Негибридные p-орбитали атомов углерода (по одной у каждого атома)
расположены перпендикулярно к плоскости молекулы и перекрываются не только
между атомами 1,2 и 3,4, но и между атомами 2,3. Электроны на таких орбиталях образуют
общую p-электронную систему однако перекрывание p-орбиталей между атомами углерода 2 и 3 менее
полное, чем 1,2- и 3,4-перекрывание.
3. Гомологический
ряд
Общая формула диеновых
углеводородов CnH2n-2
C3H4 – пропадиен
C4H6 – бутадиен
C5H8 – пентадиен
C6H10 – гексадиен
C7H12 – гептадиен
C8H14 – октадиен
C9H16 – нонадиен
C10H18 – декадиен
4. Изомерия
I. Структурная:
а) C-скелет:
CH2 =
CH – CH = CH – CH3 CH2
= CH – C = CH2
петадииен-1,3 |
CH3
2-метилбутадиен-1,3
б) двойная связь
CH2 =
CH – CH = CH – CH3 CH2
= C = CH – CH2 – CH3
пентадиен-1,3
пентадиен-1,2
в) межклассовая (с алкинами)
C3H4 C3H4
CH º C – CH3
CH2 = C = CH2
II. Пространственная
CH3 – CH = CH – CH = CH2
H H CH3
H
| | | |
C = C C
= C
| | | |
CH3 CH=CH2 H
CH=CH2
циспентодиен-2,4 транспентодиен-2,4
5. Свойства
а) физические
Бутадиен-1,3 (Дивинил)– бесцветный газ с неприятным
запахом, температурой плавления –4,5°C. Практически нерастворим в воде.
2-Метилбутадиен-1,3 (Изопрен) – при обычных условиях –
жидкость с температурой кипения 34°C.
б) химические
1.
Гидрирование и галогенирование
Алкаднены могут присоединять
водород (в момент выделения, т е. водород в виде атомов Н) и галогены. Обычно
атомы водорода или галогена присоединяются к атомам углерода, занимающим в цепи
положения 1 и 4 (так называемое 1,4-присоединение). При этом образуется новая
двойная связь между углеродными атомами. Атомы
водорода или галогена могут присоединяться также к атомам углерода 1 и 2
(1,2-присоединение), при этом вторая двойная связь в алкадиене не изменяется.
CH2
= CH – CH = CH2 + H2 ® CH3 – CH = CH –
CH3
CH2
= CH – CH = CH2 + Br2 ® CH2Br – CH = CH
– CH2Br
2.
Гидрогалогенирование
Присоединение хлороводорода к бутадиену-1,3 приводит к
образованию продуктов 1,2- и 1,4-присоединения:
® CH2Cl – CH = CH – CH3
CH2 = CH – CH = CH2
+ HCl –|
® CH2 = CH – CHCl – CH3
3.
Полимеризация
4.
Горение
6. Получение
1.
Дегидрирование алканов
CH3
– CH2 – CH2 – CH3 ® CH2 = CH – CH =
CH2 + 2H2
2.
Реакция Лебедева (дегидрирование и дегидратация)
ZnO
и Al2O3 –
католизаторы
C2H5OH
+ C2H5OH ® CH2 = CH – CH = CH2 + 2H2O + H2
7. Применение
Алкадиены
применяются для производства каучука.
Каучук.
В современной промышленности важную роль играю
эластомеры – высокомолекулярные вещества, сохраняющие эластичность в широком
интервале температур Эластомеры легко изменяют фирму при внешнем воздействии, а
после окончания воздействия принимают исходную форму. Типичными эластомерами
являются каучуки.
Натуральный каучук.
Натуральный каучук получается из природного сырья — сока дерева гевеи,
распространенного в Южной Америке (главным образом в Бразилии). На воздухе
белый млечный сок этого дерева быстро твердеет и темнеет, превращаясь в эластичную массу.
Натуральный каучук представляет собой полимер
изопрена, его состав отвечает формуле:
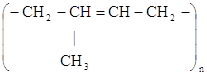
Синтетический каучук. Большие потребности промышленности в каучуке
обусловили разработку синтетических способов его получения.
В СССР синтетический каучук начал впервые
производиться в промышленных масштабах в 19321 по способу С. В. Лебедева. Этот
способ заключался в полимеризации бутадиена-1,3 в присутствии металлического натрия в качестве катализатора:
nСН2 = СН – СН =CH2 ® (– СН2 – СН = СН – СН2 –)n
бутадиен-1,3 бутадиеновый каучук
(полибуталиен)
Такой каучук уступает по свойствам натуральному: он
менее эластичен, изделия из него быстрее изнашиваются.
Каучук используют в производстве шин,
резинотехнических изделий, клеев, эбонита, медицинских и бытовых изделий.
Для превращения каучука в резину проводят вулканизацию каучука. Резина отличается от
каучука большей эластичностью и прочностью. Она устойчивее к действию
температуры и растворителей.